Fluorescencja chlorofilu
| English version is here |
Roślinny barwnik
W rzeczywistości chlorofil nie jest pojedynczą substancją, jest to raczej cała klasa związków chemicznych o podobnej budowie i właściwościach. Chlorofile są grupą organicznych związków chemicznych obecnych między innymi w roślinach, glonach i bakteriach fotosyntetyzujących. Nadają one roślinom charakterystyczny zielony kolor.
Funkcją chlorofili w organizmach przeprowadzających fotosyntezę jest wychwytywanie fotonów i przekazywanie energii spożytkowanej następnie w dalszych etapach fotosyntezy. Zielony kolor chlorofilu spowodowany jest wysoką absorpcją w czerwonej i niebieskiej części spektrum światła, a niską w zielonej części spektrum.
Wyróżnia się wiele rodzajów chlorofili. Najbardziej rozpowszechnione w przyrodzie to chlorofil a i chlorofil b występujące u wszystkich roślin przeprowadzających fotosyntezę. Chlorofile c i d występują jedynie u części glonów.
Dla przykładu przytoczę wzór strukturalny chlorofilu b:
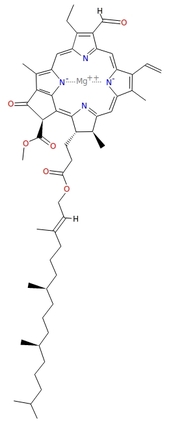
Jego wzór sumaryczny to C55H70O6N4Mg, jest to więc stosunkowo rozbudowana cząsteczka.
Dziś w prostu sposób wyizolujemy chlorofil z tkanek roślinnych, a także przekonamy się, że fluoryzuje on pod wpływem światła ultrafioletowego.
Doświadczenie
Potrzebujemy jakiegoś źródła chlorofilu. Mogą być to jakiekolwiek zielone części roślin; najbardziej nadają się mięsiste liście. W zimie z braku świeżych, zielonych roślin można w tym celu wykorzystać szpinak, choćby mrożony.
Liście trzeba najpierw pociąć na mniejsze fragmenty. Chlorofile są nierozpuszczalne w wodzie, dlatego trzeba wykorzystać inny rozpuszczalnik; odpowiedni będzie aceton C3H6O.
Ostrzeżenie: Aceton nie jest toksyczny, jest jednak klasyfikowany jako substancja drażniąca lub mogąca spowodować tymczasowe uszkodzenie zdrowia. Jest to bardzo lotna ciecz; należy unikać wdychania jej par. Autor nie bierze jakiejkolwiek odpowiedzialności za wszelkie mogące powstać szkody. Robisz to na własne ryzyko!
Fragmenty liści ucieramy w moździeżu z kilkunastoma mililitrami acetonu. W czasie tej czynności można zauważyć, że chlorofile zostaną wypłukane przez rozpuszczalnik, co objawi się przybraniem przez niego charakterystycznej, zielonej barwy. Roztwór następnie trzeba przesączyć by pozbyć się fragmentów tkanki roślinnej.
Otrzymany acetonowy roztwór chlorofili ma charakterystyczny, trawiastozielony kolor. Widać to na poniższym zdjęciu.
Czy na pewno roztwór jest zielony? W świetle widzialnym niewątpliwie tak, ale spróbujmy naszą próbkę oświetlić światłem ultrafioletowym. Wtedy widok jest zdecydowanie inny:
Pod wpływem ultrafioletu roztwór zaczyna silnie świecić na piękny, karminowoczerwony kolor. Można się o tym przekonać także oświetlając roztwór laserem półprzewodnikowym emitującym światło o długości fali λ=405nm:
W ten prosty sposób przekonaliśmy się o fluorescencyjnych właściwościach tak powszechnie występującej substancji, jaką jest chlorofil.
Wyjaśnienie
Cząsteczka każdego chlorofilu zbudowana jest z feoporfiryny, będącej pochodną porfiryny. Cztery z pierścieni to pierścienie pirolowe, a piąty pierścień tworzą same atomy węgla. Wiązania pomiędzy atomami tworzącymi pierścienie to następujące po sobie wiązania pojedyncze i podwójne składające się na układ wiązań sprzężonych.
Centralne miejsce w układzie porfiryny zajmuje atom magnezu łączący się z atomami azotu każdego z pierścieni. Porfiryna tworząca kompleks z magnezem posiada zdolność do absorpcji promieniowania elektromagnetycznego w zakresie widzialnym.
Dzięki takiej budowie cząsteczka chlorofilu może zostać także wzbudzona światłem ultrafioletowym. Wzbudzona cząsteczka posiada większą energię niż w stanie podstawowym. Stan taki jest nietrwały i po bardzo krótkim czasie następuje spontaniczne przejście do stanu podstawowego. Zgodnie z zasadą zachowania, różnica energii między tymi dwoma stanami zostaje oddana do środowiska w postaci promienistej - jest to właśnie obserwowane przez nas światło o czerwonej barwie.
Życzę miłej i pouczającej zabawy:)
Literatura dodatkowa
- Berg J.M., Tymoczko J.L., Stryer L., Clarke N.D., Szweykowska-Kulińska Z., Jarmołowski A., Augustyniak H., Biochemia, Wydawnictwo Naukowe PWN, Warszawa, 2007, str. 530
- Kopcewicz J., Lewak S., Gabryś H., Fizjologia roślin, Wydawnictwo Naukowe PWN, Warszawa, 2005
- Muyskens M., Vitz E., The Fluorescence of Lignum nephriticum: A Flash Back to the Past and a Simple Demonstration of Natural Substance Fluorescence, Journal of Chemical Education, 2006, 83(5), str. 765
Marek Ples



