Samozapłon
Silnie egzotermiczna reakcja
Reakcja egzotermiczna to reakcja chemiczna, która ma dodatni bilans wymiany ciepła z otoczeniem (przeciwieństwo reakcji endotermicznej, o której możesz przeczytać tutaj). Znaczy to, że w czasie zachodzenia reakcji jest emitowana energia cieplna. Oczywiście nie jest to jakieś chemiczne perpetuum mobile. Wytworzone ciepło pochodzi z wyzwolonej energii wiązań chemicznych. Kiedy sumaryczna energia wiązań chemicznych w produktach reakcji jest niższa niż w substratach to zgodnie z zasadą zachowania energii (energia nie może powstać z niczego ani zniknąć-możliwa jest jedynie przemiana jednej formy energii w inną) różnica ta zostanie oddana do środowiska, w tym przypadku pod postacią ciepła.
Można podać wiele przykładów reakcji egzotermicznych. Nas interesuje jej jaskrawy przykład: samozapłon. Ma on miejsce wtedy, gdy w toku reakcji egzotermicznej zostanie wytworzona wystarczająca ilość ciepła by spowodować zapłon reagentów. Obserwujemy wtedy zapłon mieszaniny reakcyjnej pomimo braku dopływu energii z zewnątrz.
Co musimy zgromadzić?
Musimy posiadać następujące składniki:
- glicerynę,
- nadmanganian potasu, inaczej manganian(VII) potasu, o wzorze KMnO4
Oba odczynniki możemy nabyć w aptece. Czasami trzeba popytać w paru, ale w końcu się trafia. Nadmanganian potasu jest używany jako środek dezynfekujący wodę; gliceryna ma wiele różnorodnych zastosowań. Mając oba składniki możemy przystąpić do doświadczenia.
Ostrzeżenie: W reakcji występuje otwarty ogień i mogą odpryskiwać na boki krople rozgrzanej mieszaniny reakcyjnej. Należy zachować bezwzględną ostrożność. Z powodu wydzielających się gazów doświadczenie można przeprowadzić jedynie na zewnątrz lub pod sprawnie działającym dygestorium. Należy także uważać na nadmanganian. Jest to bardzo silny barwnik: w kontakcie z wilgotną skórą może postawiać bardzo trudne do usunięcia fioletowe plamy. Autor nie bierze jakiejkolwiek odpowiedzialności za wszelkie mogące powstać szkody. Robisz to na własne ryzyko!
Przygotowanie
Musimy przygotować płytkę lub podstawę wykonaną z ognioodpornego materiału. Dobrze nadaje się płytka azbestowa (uważać - material ten jest rakotwórczy!) lub płytka ceramiczna. Ja wykorzystuję płytkę ceramiczną pozostałą po kafelkowaniu łazienki. Na płytkę kładziemy arkusik papieru. Na nim usypujemy niewielki kopczyk nadmanganianu. W jego szczycie dobrze jest zrobić niewielkie zagłębienie. Następnie do zagłębienia na szczycie kopczyka wkraplamy delikatnie parę kropel gliceryny i odsuwamy się na bezpieczną odległość. Po kilkudziesięciu sekundach mieszanina gwałtownie się zapala. Całość możemy zobaczyć poniżej:
Dlaczego?
Zachodzącą reakcję można zilustrować równaniem:
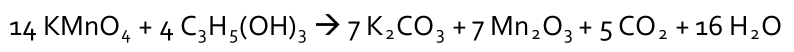
Nadmanganian potasu jest silnym utleniaczem. Początkowo utlenia on względnie powoli glicerynę, która jest trójwodorotlenowym alkoholem. W tym procesie wydziela się ciepło, które podgrzewa środowisko reakcji. Reakcja ta zachodzi szybciej w wyższej temperaturze, więc cały proces ulega gwałtownemu przyspieszeniu. W efekcie powoduje to zapłon substratów. Gliceryna zostaje utleniona głównie do dwutlenku węgla i wody.
Życzę miłej i pouczającej zabawy:)
Literatura dodatkowa:
- Bowes P. C., Self-heating: Evaluating and Controlling the Hazards, Department of the Environment, Building Research Establishment, London, 1984,
- Kreißl F. R., Krätz O., Feuer und Flamme, Schall und Rauch, Wiley-VCH, Weinheim, 2008.
Marek Ples
