Genialny roztwór w labiryncie
| English version is here |
Poniższy artykuł został opublikowany pierwotnie w czasopiśmie dla nauczycieli Chemia w Szkole (4/2021):


Labiryntem nazywamy zwykle strukturę, klasycznie np. w postaci budowli, odznaczająca się zawiłym układem dużej liczby pomieszczeń i łączących je korytarzy. Rolę labiryntu mogą pełnić też zmniejszone modele tego rodzaju budowli. Budowle takie były znane i budowane już w czasach starożytnych - między innymi w starożytnej Mezopotamii i Egipcie, gdzie znalazł zastosowanie jako zabezpieczenie oraz utrudnienie dostępu do bogato zdobionych, a często także wypełnionych kosztownościami grobowców. W sztuce greckiej i rzymskiej wyobrażenia labiryntu - często symboliczne i mocno stylizowane - występowały powszechnie w malarstwie wazowym, na mozaikach i monetach.
Jednym z najczęściej opisywanych labiryntów jest ten, który miał zostać zbudowany przez Dedala - znanego nam z mitów greckich architekta i wynalazcy. Według przekazu budowla ta wznosiła się w Knossos na Krecie i służyła uwięzieniu Minotaura, czyli potwora zazwyczaj przedstawianego jako olbrzyma z głową byka.
Motyw labiryntu został też zaadoptowany jako motyw zdobniczy o skomplikowanym, najczęściej spiralnym lub meandrowym kształcie. W gotyckich katedrach takie labirynty były często układane na posadzkach katedr. Labirynt z XII wieku można zobaczyć w katedrze w Chartres w północnej Francji. Nie były one jedynie ozdobą i miały pewne znaczenie praktyczne: przebycie skomplikowanej drogi wyznaczonej na podłodze świątyni zastępowało w funkcji podjęcie pielgrzymki.
Labirynty, tak jak i dawniej, tworzy się także dziś jako atrakcję lub formę rozrywki, np. w parkach i ogrodach poprzez odpowiednie nasadzenie i uformowanie różnorodnych roślin jako żywopłotów.
Skomplikowana struktura labiryntu znalazła pewne znaczenie jako forma łamigłówki, ale także jako test zdolności rozwiązywania szczególnych problemów. Dlatego też większości z nas nie jest obce wyobrażenie pewnych doświadczeń biologicznych polegających na umieszczeniu w labiryncie zwierząt: myszy, szczurów, świnek morskich i innych. Eksperymenty tego rodzaju były rzeczywiście prowadzone w przeszłości, co znajduje czasem kontynuację w badaniach współczesnych. Sam opisałem pewne nieskomplikowane doświadczenia z zakresu neurobiologii i behawioryzmu możliwe do przeprowadzenia w warunkach szkolnej pracowni – ich obiektem był prosionek szorstki Porcellio scaber [1].

Rozwiązanie problemu pokonania labiryntu jak najkrótszą drogą nie jest wcale trywialne i badań nad nim podjęło się wielu naukowców z różnych dziedzin, między innymi cybernetyki. Pierwszym praktycznym rozwiązaniem tego zadania był automat zbudowany w 1953 roku przez amerykańskiego pioniera cybernetyki Claude’a Elwooda Shannona i zwany przez innych myszą Shannona, a przez samego wynalazcę Tezeuszem. Urządzenie składało się z trzech zasadniczych części: labiryntu z poruszającą się w nim makietą myszy, układu elektromagnetycznego kierującego ruchami myszy oraz układu pamięciowego opartego na przekaźnikach elektromechanicznych. Tezeusz demonstrował pewne podpatrzone w naturze mechanizmy działania pamięci, a także pokazywał w praktyce możliwość zbudowania urządzenia posiadającego zdolność do uczenia się metodą prób i błędów.
Dziś problemy labiryntowe i pokrewne nie straciły wcale na aktualności (wystarczy sobie wyobrazić jak zawiła sieć powiązań łączy elementy dzisiejszej globalnej sieci internetowej) są rozwiązywane zazwyczaj przez odpowiednie programy komputerowe.
Zanim przejdziemy do dalszej części artykułu chciałbym jednak przywołać cytat z „Dzienników Gwiazdowych” Stanisława Lema, gdzie w czasie Podróży Dwudziestej Pierwszej bohater w osobie Ijona Tichego trafia na Dychtonię. Mieszkańcy tej planety poczynili tak wielkie postępy w dziedzinie rozwoju sztucznych form myślenia, że byli zdolni produkować „świadomości i psychiki w płynach; syntetyzowano mądre i myślące roztwory, które można było butelkować, rozlewać, zlewać, a za każdym razem powstawała osobowość, nieraz bardziej uduchowiona i mądrzejsza niż wszyscy Dychtończycy razem wzięci” [2].
Śmiała myśl Pisarza tak daleko wybiegła w niezbadane przez nas jeszcze rejony nauki, że nawet trudno nam sobie wyobrazić sposób realizacji idei takiego myślącego roztworu. Z całą odpowiedzialnością mogę jednak stwierdzić, że po lekturze niniejszego artykułu będziesz mógł, mój Szanowny Czytelniku, wytworzyć roztwór (czy raczej pewien układ reakcyjny) wykazujący w odpowiednich warunkach zdolność do znalezienia w labiryncie drogi od startu do mety. Co więcej, będzie to zawsze droga najkrótsza! Może więc nie będzie to tak genialny płyn jak ten opisany przez Lema, ale efekty doświadczenia mogą być dowodem, że sztuczny system przetwarzający informację (a więc w jakimś przynajmniej ograniczonym sensie inteligentny) niekoniecznie musi przyjmować formę urządzenia elektronicznego lub programu komputerowego, ale np. nieskomplikowanego układu fizyko-chemicznego, tak jak w opisanym przypadku.
Doświadczenie
Aby wykonać doświadczenie musimy zgromadzić substancje z poniższej listy:
- wodorotlenek potasu KOH (możliwy do zastąpienia wodorotlenkiem sodu NaOH),
- kwas oleinowy C17H33COOH,
- kwas chlorowodorowy HCl(aq),
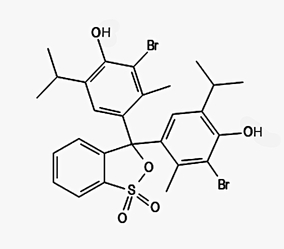
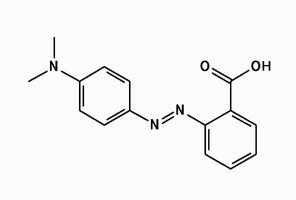
- barwnik, np. błękit bromotymolowy C27H28Br2O5S lub czerwień metylowa C15H15N3O2.
- agar-agar (niekonieczny, ale przydatny).
Kwas oleinowy jest organicznym związkiem chemicznym z grupy jednonienasyconych kwasów tłuszczowych, może być traktowany jako cis-izomer kwasu elaidynowego. W warunkach normalnych ma postać bezbarwnej cieczy, żółknącej, a następnie ciemniejącej na powietrzu (Fot.1).
Substancja ta występuje naturalnie w tłuszczach i jest głównym składnikiem oliwy z oliwek oraz tranu [3]. Dzięki posiadaniu w swojej strukturze wiązania podwójnego, kwas oleinowy może poprzez katalityczne uwodornienie zostać przeprowadzony w kwas stearynowy, co nosi nazwę utwardzania tłuszczu. Jest używany do produkcji smarów i środków piorących.
Kwas oleinowy nie jest silną trucizną, ale w przypadku pozostałych substancji konieczna jest ostrożność. Zarówno wodorotlenek sodu i kwas chlorowodorowy, jak i ich roztwory są żrące – mogą powodować dotkliwe i trudno gojące się oparzenia. Jeśli chodzi o błękit bromotymolowy (Rys.1) i czerwień metylową (Rys.2), to podejrzewa się je o właściwości rakotwórcze. Jak zawsze podczas pracy w laboratorium musimy zachować ostrożność i stosować odpowiednie środki ochrony osobistej.
W celu przeprowadzenia doświadczenia musimy zbudować też odpowiedni labirynt. Korytarze, czy raczej kanały powinny być stosunkowo wąskie, o szerokości około 1-2mm. Można oczywiście wykonać taki labirynt różnymi metodami, np. poprzez frezowanie lub po prostu wydrapanie odpowiednich ścieżek w jakimś tworzywie sztucznym, ale wyjątkowo przydatną w tym celu techniką jest druk przestrzenny.
Zastosowałem jedną z drukarek 3D działających w oparciu o metodę FDM (ang. fused deposition modelling) czyli osadzania stopionego materiału. Tego rodzaju urządzenia do użytku domowego i amatorskiego są jak najbardziej dostępne, tak jeśli chodzi o kupno gotowych urządzeń, jak i ich samodzielną budowę. Dodatkowo, korzystając z przyznawanych funduszy wiele szkół i pracowni uczelnianych zaopatrzyło się w drukarki tego typu. W metodzie FDM nanoszony materiał przeciskany jest przez dyszę ogrzaną do temperatury jego topnienia. Plastyczne tworzywo jest następnie układane warstwa po warstwie, dzięki czemu powstaje przestrzenny obiekt.
W swoich doświadczeniach wykorzystałem specyficzne tworzywo, jakim jest polilaktyd PLA będący z chemicznego punktu widzenia poli(kwasem mlekowym) o strukturze meru −[−CH(CH3)C(O)O−]−. Tworzywo to jest pełni biodegradowalne, a wytwarza się je z odnawialnych surowców w rodzaju np. mączki kukurydzianej. Wykorzystanie polilaktydu obejmuje także cele biomedyczne.
Rozkład PLA przyspiesza ekspozycja na światło UV, wilgoć i inne czynniki. Dlatego wykonane z niego sprzęty należy przechowywać w odpowiednich warunkach, jeśli mają służyć nam przez dłuższy czas. Oczywiście ten sam projekt można wykonać z innych, nie biodegradowalnych materiałów. Wymaga to jednak zmiany warunków druku 3D.
Labirynt zaprojektowałem w programie FreeCAD (wer. 0.19.2), a następnie wyeksportowałem do formatu *.stl, który jest akceptowany przez większość aplikacji obsługujące drukarki przestrzenne. Fot.2 obrazuje projekt labiryntu, ukazany w edytorze grafiki trójwymiarowej Blender (wer. 2.93.1). Obie aplikacje są przykładami wolnego i otwartego oprogramowania więc nic nie stoi na przeszkodzie, aby każdy mógł stworzyć swój własny projekt. Do pierwszych doświadczeń dla chętnych udostępniam plik z labiryntem opisanym w artykule (do pobrania tutaj).
Parametry wydruku ustawiono na standardowe dla tworzywa PLA – wybrano biały polikaktyd, dla większej przejrzystości. Zastosowano dyszę 0,4mm przy grubości warstwy 0,2mm. Większa dokładność nie jest tutaj konieczna. Wydruk należy wyskalować odpowiednio do swoich potrzeb - w moim przypadku długość jego boku wyniosła 55mm. Sam proces druku zajął kilkadziesiąt minut, po czym uzyskano gotowy model labiryntu odpowiedni do wykorzystania w doświadczeniu (Fot.3).
Jak widać, labirynt nie jest skomplikowany, ale zobaczymy jak z nim sobie poradzi nasz roztwór.
Przydatną w doświadczeniu rzeczą jest przygotowanie żelu przez rozmieszanie niewielkiej ilości (2% wagowo) agar-agaru we wrzącej wodzie destylowanej. Uzyskany żel łatwo krzepnie w temperaturze pokojowej po wylaniu np. do szalek Petriego, skąd łatwo następnie wydostać żelowe krążki (Fot.4).
Krążki trzeba później pociąć na niewielkie fragmenty (mieszczące się na polu mety labiryntu), po czym powinny zostać przeniesione do roztworu kwasu chlorowodorowego o stężeniu około 3,7%, gdzie powinny pozostać kilka godzin (Fot.5).
W razie braku agaru nie ma się co załamywać – podobną rolę spełni np. niewielki fragment gąbki lub tkaniny nasączony kwasem o podanym stężeniu.
Przystępując do doświadczenia musimy przygotować też roztwór roboczy, poprzez rozpuszczenie w 100cm3 destylowanej wody najpierw 0,28g wodorotlenku potasu, a następnie około 0,2cm3 kwasu oleinowego, co może wymagać dosyć energicznego mieszania. Roztwór ma postać przejrzystej, bezbarwnej i łatwo pieniącej się cieczy (Fot.6).
Model labiryntu należy ustawić jak najdokładniej poziomo i następnie wypełnić wszystkie korytarze do połowy wysokości przygotowanym przed chwilą roztworem (Fot.7A).
Po wypełnieniu labiryntu roztworem w komorze stanowiącej wyjście z labiryntu albo jego metę (oznaczonej jako M) należy umieścić bloczek agaru nasączony kwasem chlorowodorowym, po czym szybko do komory startowej S przenieść szpatułką niewielką ilość stałego barwnika – w tym przypadku błękitu bromotymolowego (Fot.7B). Trzeba to zrobić w taki sposób aby barwnik rozpływał się po powierzchni cieczy, na granicy faz. Już po chwili można zauważyć, że zamiast rozprzestrzeniać się bezładnie, barwna smuga płynie najkrótszą drogą do mety (Fot.7C). Możemy też zauważyć, że smuga zmienia swą barwę, od początkowo niebieskiej, przez zielonkawą, aż do żółtej w pobliżu końca swojej drogi.

Błękit bromotymolowy możemy zastąpić także innymi barwnikami, np. czerwienią metylową (Fot.8). W jej przypadku przejścia barwne (między kolorami żółtopomarańczowym a czerwonym) są jednak nieco mniej dostrzegalne.
Proces można prześledzić dokładniej na sekwencji obrazów – wykorzystano tym razem nieco inny, ale podobny model labiryntu i ponownie błękit bromotymolowy (Fot.9).
Wyjaśnienie
Mechanizm obserwowanego efektu i „zdolności” układu do roziązania zadania znalezienia najkrótszej drogi w labiryncie należy się doszukiwać w zjawiskach związanych z napięciem powierzchniowym [4]. Napięciem powierzchniowym nazywamy zjawisko fizyczne występujące na granicy faz, a więc na styku powierzchni cieczy z ciałem stałym, gazem lub inną cieczą. W jego efekcie powierzchnia ta zachowuje się jak elastyczna błonka pokrywająca ciecz. W ujęciu ilościowym jest to energia przypadająca na jednostkę powierzchni, co jest równoważne pracy potrzebnej do powiększenia powierzchni o tę jednostkę. Występowanie napięcia powierzchniowego tłumaczy się istnieniem sił przyciągania pomiędzy cząstkami cieczy. Wysokie napięcie powierzchniowe na granicy faz oznacza, że siły kohezji w obrębie faz są większe niż siły adhezji na granicy tych faz.
Wartość napięcia powierzchniowego zależy od wielu czynników. Jednym z nich jest obecność pewnych związków chemicznych nazywanych substancjami powierzchniowo czynnymi. Cząsteczki tych substancji gromadzą się na granicy faz ułatwiając ich kontakt. Są one zbudowane z dwóch części, z których każda odpowiada za łatwe mieszanie się z odrębną fazą. Cząsteczka substancji powierzchniowo czynnej zmniejszającej napięcie międzyfazowe na granicy wody i powietrza musi zawierać fragment hydrofilowy, wykazujący powinowactwo z wodą (dzięki swojej polarności), oraz fragment hydrofobowy, o zdecydowanie niższym powinowactwie do wody, a więc zwykle o niepolarnym charakterze.
Z napięciem powierzchniowym, czy raczej z jego różnicami, jest związanych wiele zjawisk fizycznych – jednym z nich jest efekt Marangoniego. Polega on na powierzchniowym przepływie cieczy w kierunku od niższego napięcia powierzchniowego do wyższego, co możemy zaobserwować nanosząc kroplę mydła na powierzchnię cieczy posypanej np. talkiem lub pieprzem – gwałtowny „odskok”drobin unoszących się na powierzchni cieczy jest spowodowany właśnie znacznym lokalnym zmniejszeniem napięcia powierzchniowego przez środek powierzchniowo czynny [5].
W naszym przypadku, podczas roztwarzania kwasu oleinowego (opisanego dalej symbolicznie jako HR, R oznacza resztę kwasu oleinowego) w zasadowym roztworze spowodowaliśmy jego deprotonację w myśl równania:
Reakcja jest odwracalna, a jej równowaga zależy od odczynu środowiska – w zasadowym przeważa reakcja deprotonacji, zaś w kwasowym protonacji.
Powstałe w ten sposób jony oleinianowe R− posiadając zarówno polarną „głowę” obdarzoną zlokalizowanym ładunkiem ujemnym (fragment hydrofilowy), jak i długi niepolarny "ogon" czyli łańcuch węglowodorowy (fragment hydrofobowy) stanowią doskonały środek powierzchniowo czynny. Grupują się one na granicy faz roztwór-powietrze zmniejszając tym samym wartość napięcia powierzchniowego. Można to stwierdzić choćby po skłonności do pienienia się roztworu (vide Fot.6).
Wypełniając labirynt tak przygotowanym roztworem zapewniamy jednorodną wartość napięcia powierzchniowego na całej powierzchni kanałów.
Wprowadzając w określonym miejscu startowym S labiryntu bloczek agaru nasączonego kwasem zmieniamy jednak równowagę kwasowo-zasadową układu, przy czym w obrębie kanałów powstaje charakterystyczny gradient pH rosnącego od miejsc bardziej odległych mecie w jej kierunku. Krótko mówiąc: im bliżej mety M, tym roztwór wypełniający kanały jest bardziej kwaśny.
Zauważmy, że skoro przeważający kierunek przytoczonej wcześnie reakcji zależy od środowiska, przez co w obrębie labiryntu powstał gradient pH, to także równowaga wspomnianej reakcji będzie odwzorowywała wskazaną zależność. Dzięki temu w rejonach labiryntu bliższych miejscu startowemu S koncentracja formy zdeprotonowanej kwasu oleinowego będzie najwyższa. Zbliżając się natomiast do mety M moglibyśmy zanotować jej spadek na rzecz wzrostu koncentracji formy sprotonowanej.
Biorąc pod uwagę działanie powierzchniowo czynne formy zdeprotonowanej łatwo już wysnuć wniosek, że także rozkład wartości napięcia powierzchniowego w labiryncie stanie się niejednakowy: będzie ono rosło w kierunku od startu do mety. Na skutek efektu Marangoniego powstanie więc powierzchniowy przepływ cieczy unoszący cząstki barwnika znaczące najkrótszą drogę łączącą punkt dodania barwnika i miejsce umieszczenia zakwaszonego bloczku. Zauważmy, że przepływ we wskazanym kierunku odbywa się jedynie na powierzchni – w głębi cieczy (przy dnie kanału) płynie ona przeciwnie. Właśnie dlatego dla powodzenia doświadczenia konieczna jest odpowiednia aplikacja barwnika.
Zmiany barwy smugi wskazującej drogę w labiryncie – jako że użyliśmy wskaźników pH – odwzorowują gradient odczynu środowiska.
Warto zauważyć, że z racji opisanego mechanizmu w przypadku jeśli w labiryncie istnieją dwie możliwe drogi, to barwna smuga jako pierwszą pokona tę krótszą.
Literatura:
- [1] Ples M., W labiryncie - decyzje równonoga, Biologia w Szkole, 4 (2019), Forum Media Polska Sp. z o.o., str. 56-62 powrót
- [2] Lem S., Dzienniki Gwiazdowe, Czytelnik, Warszawa, 1976, str. 235 powrót
- [3] Hassa R., Mrzigod J., Podręczny słownik chemiczny, Videograf II, Katowice, 2004, str. 213 powrót
- [4] Suzuno K., Ueyama D., Branicki M., Tóth R., Braun A., Lagzi I., Maze Solving Using Fatty Acid Chemistry, Langmuir, 2014, 30(31), str. 9251-9255 powrót
- [5] Thomson J., On certain curious Motions observable at the Surfaces of Wine and other Alcoholic Liquors, Edinburgh and Dublin Philosophical Magazine and Journal of Science, Londyn, 1855, str. 330-333 powrót
Wszystkie fotografie i rysunki zostały wykonane przez autora
Marek Ples








