Roślinne trucizny - alkaloidy i ich wykrywanie
Poniższy artykuł został opublikowany pierwotnie w czasopiśmie dla nauczycieli Biologia w Szkole (2/2018):

Myślę, że nie będzie przesady w stwierdzeniu, że rośliny stanowią podstawę istnienia życia na Ziemi - bez nich bowiem nie mogłaby istnieć większość innych organizmów. Właściwie prawie cała dostępna nam energia pochodzi bezpośrednio lub pośrednio ze Słońca. Fotosynteza jest więc podstawowym źródłem energii i materii organicznej w zdecydowanej większości ekosystemów. Dla dużej części organizmów zwierzęcych rośliny stanowią ważne lub nawet jedyne źródło pokarmu.
Poza tlenem i pożywieniem organizmy roślinne dostarczają nam przydatnych surowców, m.in. drewna, włókien i innych materiałów. Rośliny produkują wiele różnych substancji chemicznych. Jednym z ich rodzajów są alkaloidy.
Nazwą tą określa się grupę naturalnie występujących (głównie w roślinach) zasadowych, najczęściej heterocyklicznych związków organicznych zawierających w swojej strukturze azot. Trzeba jednak pamiętać, że aminokwasy, peptydy, białka, nukleotydy, kwasy nukleinowe, antybiotyki i aminocukry zwykle nie są zaliczane do tej grupy. Niektóre związki obojętne związane w jakiś sposób z alkaloidami zasadowymi są także włączane do alkaloidów [1].
Biorąc pod uwagę zawartość azotu w alkaloidach nie zaskakuje fakt, że punktem wyjściowym ich biosyntezy są aminokwasy. Prawie wszystkie alkaloidy są w normalnych warunkach ciałami stałymi - występowanie w postaci cieczy należy tu do wyjątków. Są słabo rozpuszczalne w wodzie, za to doskonale w wielu rozpuszczalnikach organicznych.
Cechą charakterystyczną omawianych związków jest wykazywanie silnego, często toksycznego działania fizjologicznego na organizmy zwierzęce. Jest to wykorzystywane przez człowieka, ponieważ wiele alkaloidów podawanych w odpowiednich dawkach stanowi skuteczne leki na liczne choroby i dolegliwości - przykładem może być tu chinina czy kodeina. Trzeba też wspomnieć, że alkaloidy stanowią składniki wielu dozwolonych używek (kofeina, teobromina, nikotyna), ale też narkotyków takich jak kokaina. Niektóre z szczególnie silnie toksycznych alkaloidów znajdują zastosowanie jako trutki w zwalczaniu szkodników (strychnina).
Opracowano wiele sposobów wykrywania alkaloidów. Z powodu braku przyzwolenia na produkcję lub posiadanie niektórych substancji psychoaktywnych z tej grupy wspomniane metody znajdują często zastosowanie w procedurach śledczych. W niniejszym artykule chciałbym przedstawić stosunkowo proste i mało uciążliwe metody wykrywania alkaloidów. Aby bez kłopotu móc powtórzyć te doświadczenia w warunkach laboratorium szkolnego lub uczelnianego wybrałem takie sposoby, które obok zakazanych substancji pozwalają także na stwierdzenie obecności ogólnodostępnych alkaloidów.
Doświadczenie
Spośród wielu zróżnicowanych metod wykrywania alkaloidów wybrałem tą wykorzystującą tzw. odczynnik Dragendorffa. Został on wynaleziony w XIX wieku przez niemieckiego chemika Johanna Georga Noëla Dragendorffa, profesora farmacji na Uniwersytecie w Dorpacie. Odczynnik ten nie jest silnie toksyczny ani żrący.
Do przygotowania odczynnika potrzebujemy następujących substancji [2]:
- azotan(V) bizmutu(III) Bi(NO3)3,
- jodek potasu KI,
- kwas chlorowodorowy HCl 36%.
Zwykle do otrzymywania odczynnika wykorzystuje się kwas winowy C4H6O6, lecz w tym przypadku obejdziemy się bez niego.
Azotan(V) bizmutu(III) to nieorganiczny związek chemiczny, sól kwasu azotowego(V) i bizmutu na trzecim stopniu utlenienia. Z wodnego roztworu krystalizuje w postaci pentahydratu (Fot.1). W wyniku ogrzewania przekształca się w azotan bizmutylu BiONO3. Azotan(V) bizmutu(III) może mieć działanie drażniące, wykazuje silne właściwości utleniające - należy więc zachować ostrożność.
Jodek potasu jest m.in. składnikiem płynu Lugola (czyli wodnego roztworu jodu w jodku potasu), bywa także dodawany do soli kuchennej w celu suplementacji jodu na obszarach, w których występuje niedobór tego pierwiastka w pożywieniu.
Stężony kwas chlorowodorowy jest silnie żrący, a dodatkowo uwalnia się z niego gazowy chlorowodór o duszącym zapachu. Gaz ten w większych ilościach jest toksyczny. Należy zachować odpowiednie środki bezpieczeństwa.
Chcąc otrzymać odczynnik Dragendorffa należy uprzednio przygotować dwa roztwory:
- A – 0,4g azotanu(V) bizmutu(III) w 40cm3 wody z dodatkiem 1,5cm3 stężonego kwasu chlorowodorowego (w razie gdyby roztwór był mętny, dodać nieco więcej kwasu),
- B – 3g jodku potasu w 50cm3 wody.
W obu przypadkach należy użyć wody destylowanej. Gotowe roztwory są bezbarwne i przejrzyste (Fot.2).
Oba roztwory należy następnie zmieszać, uzupełnić wodą destylowaną do objętości równej 100cm3 i w razie wytrącenia się osadu odsączyć go po upływie około 24 godzin. Powstały w ten sposób odczynnik Dragendorffa jest dosyć trwały, można go przechowywać w ciemności w szczelnie zamkniętym naczyniu przez dłuższy czas. Ma on postać pomarańczowej cieczy (Fot.3).
Chcąc wypróbować otrzymany odczynnik potrzebujemy jakiegoś alkaloidu. Wiele występujących w naszym otoczeniu roślin produkuje tego rodzaju substancje. Jedną z nich jest cis pospolity Taxus baccata czyli gatunek wiecznie zielonego drzewa iglastego z rodziny cisowatych Taxaceae. Zasięg jego naturalnego występowania obejmuje Europę, zachodnią Azję oraz północną Afrykę. Cis jest drzewem długowiecznym i wolno rosnącym - osobniki liczące sobie ponad tysiąc lat nie należą do rzadkości. Tak zwany Cis Henrykowski rosnący w Henrykowie Lubańskim jest najstarszym drzewem w Polsce i według szacunków żyje od ponad 1200 lat [3]. Cis nie jest wybredny co do warunków środowiska i rośnie na różnych glebach i przy różnych warunkach nasłonecznienia. Drzewo ma duże znaczenie gospodarcze - jest wykorzystywane m.in. jako roślina ozdobna i lecznicza. Drewno cisu jest bardzo cenione jako twarde i trwałe, wąskosłoiste, z ciemnobrunatną twardzielą. Wśród wszystkich europejskich gatunków drewna jest najbardziej zbite, najbardziej sprężyste i najtrudniej łupiące się [4].
Cis jest rośliną silnie trującą z racji występowania w jego tkankach m.in. alkaloidów. Szkodliwe substancje są odkładane we wszystkich częściach rośliny poza osnówką nasion. Podczas manipulacji z tą rośliną trzeba zachować środki ostrożności.
Surowcem do dalszych doświadczeń będą liście cisu. Są to równowąskie igły o długości 2-3cm i szerokości 0,3cm, delikatnie zaostrzone na wierzchołku. Na pędzie są umiejscowione skrętolegle (Fot.4). Górna strona igieł jest ciemnozielona i błyszcząca, natomiast spodnia jest dużo jaśniejsza i matowa.
Zebrane igły należy pociąć na niewielkie fragmenty (Fot.5).
Pocięte igły trzeba następnie przenieść do ceramicznego moździerza i zalać wodą z dodatkiem odrobiny alkoholu etylowego (niekoniecznie, można pominąć). Przed ucieraniem warto dodać do mieszaniny także nieco czystego piasku np. kwarcowego (Fot.6). Ułatwia to rozdrobnienie twardych igieł.
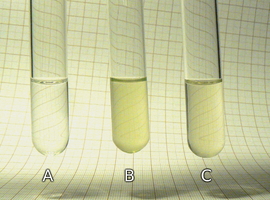
Po dokładnym roztarciu materiału roślinnego należy przesączyć powstały płyn. Do celów porównawczych dobrze jest przygotować w taki sam sposób także wyciąg z liści innej rośliny, nie zawierającej alkaloidów. Może to być np. szpinak warzywny Spinacia oleracea. Zarówno uzyskany w opisany sposób wyciąg z igieł cisa (Fot.7A), jak i z liści szpinaku (Fot.7B) jest jasnozielony.
Aby przeprowadzić test na obecność alkaloidów w wyciągach roślinnych musimy niewielkie ich ilości przenieść do probówek. Jako ślepą próbę zastosujemy wodę destylowaną (Fot.8).
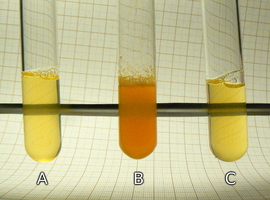
Następnie do każdej próbki dodajemy po kilka kropli odczynnika Dragendorffa i mieszamy. Wynik przedstawia Fot.9.
Powstanie zmętnienia z powodu wytrącenia osadu uważa się za wynik pozytywny próby z wykorzystaniem odczynnika Dragendorffa. Świadczy to o występowaniu w próbce alkaloidów [5].
W tkankach cisa pospolitego jest obecnych wiele trujących substancji – najważniejszą z nich jest taksyna C35H47NO10, której wzór strukturalny przedstawia Rys.1.
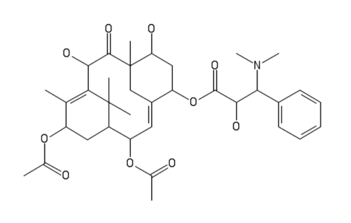
Związek ten ma negatywny wpływ na pracę serca, żołądka i jelit. W odpowiednich ilościach poraża ośrodek oddechowy, co pociąga za sobą gwałtowną śmierć [6]. Zaburza także podziały komórkowe dezorganizując proces powstawania wrzeciona kariokinetycznego.
Inną powszechnie dostępną substancją zawierającą alkaloidy jest tonik. Ten bezalkoholowy napój orzeźwiający właśnie im zawdzięcza swój charakterystyczny, gorzki smak. Aby się o tym przekonać ponownie można wykorzystać odczynnik Dragendorffa. Zaznaczę jednak, że badaną próbkę toniku najlepiej pozostawić wcześniej na jakiś czas w otwartym naczyniu, tak by przestały się z niej wydzielać pęcherzyki dwutlenku węgla CO2.
Gotowy zestaw doświadczalny przedstawia Fot.10. Próbka A zawiera nierozcieńczony tonik, próbka B tonik dziesięciokrotnie rozcieńczony wodą, natomiast próbka C wodę destylowaną. Po dodaniu odczynnika Dragendorffa można zauważyć, że bardzo wyraźne zmętnienie wystąpiło w obu próbkach zawierających tonik.
Alkaloidem zawartym w toniku jest chinina C20H24N2O2 (Rys.2).
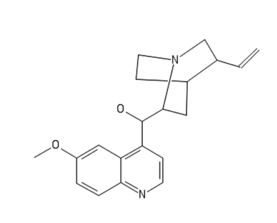
Wspomniana substancja występuje naturalnie w korze chinowca, nazywanego też drzewem chinowym Cinchona i należącego do rodziny marzanowatych Rubiaceae. Chinina była pierwszym skutecznie działającym lekiem przeciw malarii, posiada też działanie przeciwgorączkowe, przeciwzapalne i przeciwbólowe.
W Polsce i innych krajach Unii Europejskiej dopuszczalne stężenie chininy w produktach spożywczych (a więc i w toniku) wynosi do 100 miligramów na kilogram produktu. Przyjmując, że tak właśnie jest w przypadku toniku (i że jego gęstość niewiele odbiega od gęstości wody), przeliczenie ujawnia, że można go traktować jako zaledwie 0,01% roztwór chininy. Odczynnik Dragendorffa z łatwością jednak ujawnia obecność tego związku nawet przy dziesięciokrotnym rozcieńczeniu, odpowiadającemu stężeniu 0,001%. Przy dalszym rozcieńczaniu osad się w dalszym ciągu pojawia, lecz jest nieco trudniejszy do zauważenia. Doświadczenie to przekonuje nas o wielkiej czułości opisywanej metody.
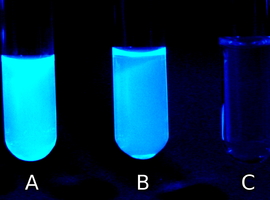
Zawartość chininy w toniku możemy wykryć także w inny, nawet bardziej spektakularny sposób. Próbki roztworów tej substancji wystarczy bowiem oświetlić promieniowaniem ultrafioletowym, by przekonać się, że bardzo intensywnie fluoryzują (Fot.11).
Jak widać, po wzbudzeniu światłem ultrafioletowym obie próbki zaczynają świecić jasnoniebieskim blaskiem (Fot.11A i B), w przeciwieństwie do wody, która pozostaje ciemna (Fot.11C). Także tę cechę chinina wykazuje nawet przy bardzo dużych rozcieńczeniach.
Kontynuując poszukiwania alkaloidów w naszym otoczeniu możemy spróbować stwierdzić ich występowanie w napojach energetyzujących. Podobnie jak w przypadku toniku próbkę takiego napoju warto pozostawić na jakiś czas w otwartym naczyniu w celu odgazowania. Fotografia 12 przedstawia wynik dodania odczynnika Dragendorffa do napoju energetycznego – stwierdzono wystąpienie bardzo silnego zmętnienia i wytrącenia się dużych ilości kłaczkowatego osadu.
W napojach tego typu występują m.in. duże ilości kofeiny C8H10N4O2 należącej do alkaloidów purynowych (Rys.3)
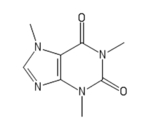
Kofeina naturalnie występuje w nasionach kawy Coffea i wielu innych surowcach pochodzenia roślinnego. Kofeina w zależności od pochodzenia bywa także nazywana teiną (z liści herbaty Camellia sinensis), guaraniną (z nasion guarany Paullinia cupana) lub mateiną (z liści lub pędów ostrokrzewu paragwajskego Ilex paraguariensis, nazywanego potocznie yerba mate). Kofeina jest stosunkowo bezpiecznym stymulantem. Należy jednak pamiętać, że w zbyt dużych dawkach jest toksyczna. Przy przyjęciu przez dorosłego, zdrowego człowieka więcej niż 0,5g występują m.in. silne pobudzenie psychoruchowe, przyspieszona i niemiarowa praca serca, nudności, wymioty i osłabienie. W skrajnych przypadkach mogą wystąpić drgawki i porażenie ośrodka oddechowego. Dawkę śmiertelną stanowi około 10g - bezpośrednim powodem śmierci jest wtedy najczęściej wystąpienie migotania komór serca [7].
W przypadku badanego napoju ilość osadu powstałego w wyniku próby Dragendorffa była tak duża, że po pewnym czasie opadł na dno probówki formując grubą warstwę (Fot.13).
Próbę z odczynnikiem Dragendorffa można też wykonać inaczej, co jest szczególnie wygodne w przypadku posiadania niewielkich ilosci badanej substancji. Wykorzystuje się w tym celu specjalną płytkę z zagłębieniami lub płytę szklaną – w tym drugim przypadku pod spodem należy umieścić czarny papier, ponieważ ułatwia to obserwację (Fot.14A). Na płycie trzeba umieścić obok siebie kroplę badanej substancji (a) i odczynnika Dragendorffa (b). Krople należy następnie połączyć, co można zobaczyć na Fot.14B. Daje się wtedy zauważyć powstanie wyraźnie odcinającego się od tła osadu (c).
W wyżej opisywanym przypadku badaną substancją był wyciąg zawierający znaną nam już kofeinę.
Podobne doświadczenia można przeprowadzić z wieloma innymi substancjami. Trzeba jednak pamiętać, że wiele alkaloidów jest bardzo silnie trujących, a posiadanie i wykorzystywanie niektórych z nich jest zabronione przez prawo.
Wyjaśnienie
By wyjaśnić sposób w jaki odczynnik Dragendorffa pozwala na wykrywanie alkaloidów musimy się nieco zastanowić nad ich właściwościami chemicznymi. Są one przeważnie zasadowe, o czym mówi już ich sama nazwa pochodząca od arabskiego alkali oznaczającego potaż i greckiego εἶδος (eidos), czyli postać. Słowo alkaloid można więc przetłumaczyć jako "przyjmujący postać zasady". Związki te w większości należą do klasy amin trzeciorzędowych. Dzięki temu mogą reagować z jodobizmutanem potasu, dając barwne pochodne. Są one nierozpuszczalne w wodzie, wytrącają się więc jako osady o barwach od żółtej do czerwonej, a czasem nawet brązowej.
Oczywiście poza odczynnikiem Dragendorffa znamy też wiele innych metod wykrywania alkaloidów, ich pochodnych oraz wielu innych substancji. Dobrze wspomnieć tutaj o odczynniku Mandelina (Fot.15A) i Marquisa (Fot.15B). Jako ciekawostkę warto powiedzieć, że obaj naukowcy, którzy opracowali wspomniane odczynniki (Karl Friedrich Mandelin i Eduard Marquis) podobnie jak Dragendorff byli związani z Uniwersytetem w Dorpacie.
Zarówno odczynnik Mandelina, jak i Marquisa pozwala nie tylko na stwierdzenie występowania określonej klasy substancji, ale także na określenie konkretnego związku chemicznego. Niestety przygotowanie obu roztworów wiąże się z operowaniem silnie żrącym stężonym kwasem siarkowym(VI) H2SO4, trudno więc polecić je do zastosowań szkolnych.
Z fizjologicznego punktu widzenia alkaloidy nie biorą czynnego udziału w metabolizmie komórki. Z tego powodu bywają określane jako substancje odpadowe. Takie podejście jest jednak często krytykowane, ponieważ produkcja alkaloidów jest z punktu widzenia ustroju bardzo kosztowna energetycznie, a dodatkowo wymaga wykorzystania azotu, który jest trudny do pozyskania ze środowiska. Trudno więc wyobrazić sobie procesy ewolucyjne dażące do tak bezcelowego trwonienia energii. Z drugiej strony, największa koncentracja alkaloidów u produkujących je roślin występuje zwykle w tkankach najbardziej podatnych na ataki roślinożerców. Tak więc hipoteza, że alkaloidy stanowią rodzaj broni, czy może raczej środka odstraszającego mającego chronić roślinę przed fitofagami wydaje się zasadna.
Literatura:
- [1] Moss G. P., P. Smith A. S., Tavernier D., Glossary of class names of organic compounds and reactivity intermediates based on structure (IUPAC Recommendations 1995), Pure and Applied Chemistry, 67 (8-9), 1995, str. 1313 powrót
- [2] Ples M., Odczynnik Dragendorffa, w serwisie: http://weirdscience.eu/, dostępne online: https://weirdscience.eu/Odczynnik%20Dragendorffa%20-%20wykrywanie%20alkaloid%C3%B3w.html, [dostęp: 01.02.2018] powrót
- [3] Seneta W., Dendrologia, Państwowe Wydawnictwo Naukowe, Warszawa, 1987, str. 38 powrót
- [4] Barański M. J., Cis, w: Harnaś, 7, wyd. PTTK, Gliwice, 1981 powrót
- [5] Nayeem A. A., Khatun A., Rahman M. S., Rahman M., Evaluation of phytochemical and pharmacological properties of Mikania cordata (Asteraceae) leaves, Journal of Pharmacognosy and Phytotherapy, 3 (8), 2011, str. 118-123 powrót
- [6] Perju-Dumbravă D., Morar S., Chiroban O., Lechintan E., Cioca A., Suicidal poisoning by ingestion of Taxus Baccata leaves. Case report and literature review, Romanian Journal of Legal Medicine, 2 (21), 2013, str. 115-118 powrót
- [7] Mutschler E., Farmakologia i toksykologia, MedPharm Polska, Wrocław, 2010 powrót
Autorem fotografii i rysunków jest Marek Ples.
Marek Ples