Reakcja fotochemiczna - chlorek srebra
Początki fotografii
Fotografia jest zbiorem wielu technik, których celem jest trwałe zarejestrowanie obrazu. Ludzi od dawna fascynowała idea uwiecznienia wiernego obrazu, lecz większe osiągnięcia w tej dziedzinie datuje się dopiero od początków XIX wieku. W 1839 roku Francuz Louis Jacques Daguerre zaprezentował pierwszą udaną fotografię.
Rozwój fotografii poprzedzony został obserwacjami natury chemicznej. Już w 1556 roku Georg Fabricius zauważył, że chlorek srebra zaczernia się pod wpływem promieni słonecznych, a wiek później światłoczułość azotanu srebra zaobserwował Johann Schultze.
Podobnie jak oni w naszym dzisiejszym doświadczeniu wykorzystamy związki srebra.
Laboratorium archaicznego fotoamatora
Ostrzeżenie: Wszystkie związki metali ciężkich są trujące. Po przeprowadzeniu doświadczenia zaleca się wypicie mleka - występujące w nim białka opłaszczają atomy metali ciężkich pozwalając organizmowi na ich usunięcie. Azotan srebra ma działanie żrące na tkanki oraz pozostawia trudne do usunięcia czarne plamy na skórze. Autor nie bierze jakiejkolwiek odpowiedzialności za wszelkie mogące powstać szkody. Robisz to na własne ryzyko!
Nie obejdzie się bez zdobycia dwóch odczynników. Jednym z nich jest chlorek sodu czyli zwykła sól kuchenna. Zdobycie drugiego może być nieco trudniejsze, ponieważ jest to azotan(V) srebra.
Azotan srebra był zwany przez dawnych alchemików kamieniem piekielnym lub lapis infernalis. Jest solą kwasu azotowego(V) i srebra. Ma postać bezbarwnych kryształów. Jak na sól srebra bardzo dobrze rozpuszcza się w wodzie. Azotan srebra łatwo rozkłada się pod wpływem światła - dlatego musi być przechowywany w naczyniu z ciemnego szkła.
Ostrzeżenie: lapis w zetknięciu ze skórą i po wystawieniu na światło tworzy niemożliwe do zmycia plamy krystalicznego srebra (znikają po kilku dniach wraz z łuszczącym się naskórkiem):

Z tego względu wszelkie manipulacje z tym związkiem należy wykonywać w odpowiednich rękawiczkach ochronnych (do nabycia w aptekach).
Następnie musimy przygotować roztwór azotanu: odważamy około 0,5 grama tego związku i rozpuszczamy w około 25 mililitrach wody destylowanej. Koniecznie należy użyć wody destylowanej lub przynajmniej demineralizowanej ponieważ woda wodociągowa jest zanieczyszczona w różnego rodzaju chlorki. Lapis zareagowałby z nimi dając osad. Musimy przygotować też stężony roztwór chlorku sodu.
Od tego momentu wszystkie czynności należy przeprowadzać przy przyćmionym świetle, lub najlepiej przy czerwonym świetle lampy ciemniowej.
Dodajemy powoli kroplami roztwór chlorku sodu do azotanu srebra. Zachodzi reakcja:
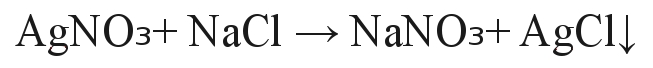
Reakcja jest dosyć widowiskowa, ponieważ roztwory obu substratów są bezbarwne i przezroczyste. W ich zetknięciu powstaje jednak wyraźnie odcinający się biały osad chlorku srebra.
W jej wyniku powstaje serowaty osad nierozpuszczalnego chlorku srebra o barwie mlecznobiałej. Soli dodajemy do momentu kiedy osad przestanie się tworzyć. Chlorek srebra po chwili opada na dno zlewki.
Należy go kilkakrotnie przemyć przez dekantację wodą destylowaną, a potem odsączyć. Wciąż mokrą substancję za pomocą bagietki rozprowadzamy na kawałku białego papieru. Ważne jest to by warstwa była jednolita. Następnie układamy na niej jakiś przedmiot - ja użyłem żyletki:
Tak przygotowany arkusik wystawiamy teraz na światło słoneczne. Po kilku minutach powierzchnia chlorku sciemnieje. Usunięcie żyletki uwidacznia nam, że papier ściemniał tylko w miejscach, do których dostęp miało światło słoneczne! Dzięki temu wyraźnie widać kontur żyletki.
Stało się tak dlatego, że chlorek srebra jest względnie trwały chemicznie tylko w ciemności. Dzięki dopływowi energii promienistej w postaci światła słonecznego zachodzi reakcja rozkładu AgCl.
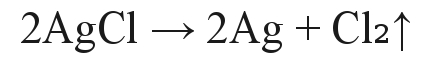
W wyniku reakcji powstaje gazowy chlor, który ulatnia się. Drugim produktem jest metaliczne srebro. Bardzo silnie rozdrobnione srebro ma barwę czarną i to ono jest odpowiedzialne za zmianę barwy.
Życzę miłej i pouczającej zabawy:)
Literatura dodatkowa:
- Iliński M., Materiały i procesy fotograficzne, Wydawnictwo Artystyczne i Filmowe, Warszawa, 1989,
- Mees C. E. K., James T.H., The Theory of the Photographic Process, 3rd ed., The Macmillan Co., New York, 1966,
- Neblette C.B., Fundamentals of Photography, Van Norstrand Reinhold Co., Princeton, New York, 1970,
- Paśko J. R., Z chemią przez fotografię jednobarwną, Wydawnictwa Naukowo-Techniczne, Warszawa, 1989.
Marek Ples



